Гонка вооружений между бактериями и фагами, вероятно, не закончится никогда. Ни одна из сторон не выйдет из этой войны окончательным победителем. Все, на что могут рассчитывать противоборствующие лагеря — динамическое равновесие.
У ученых есть резон внимательно наблюдать за ходом бактериально-фаговых баталий и исследовать представленные на поле боя молекулярные механизмы. Например, после обнаружения системы CRISPR-Cas в генной инженерии произошел самый настоящий переворот.
В январе 2018 года израильские исследователи из Института Вейцмана сообщили в журнале Science об открытии у бактерий десяти неизвестных ранее защитных механизмов: девяти противофаговых и одного противоплазмидного. Некоторые из этих систем используют компоненты бактериальных жгутиков и конденсин-подобных комплексов. Кроме того, авторы предоставили свидетельства в пользу общности происхождения древних компонентов геномов бактерий, растений и простейших животных. Без сомнения, исследование открыло новые перспективы для редактирования бактериального генома.
КАК УСТРОЕН «ИММУНИТЕТ» БАКТЕРИЙ?
Прокариоты используют разные механизмы противофаговой и противоплазмидной защиты. Одни из них изучены достаточно хорошо, другие открыли недавно и только начали исследовать.
Система адаптивной защиты CRISPR-Cas
Состоит из коротких палиндромных повторов, регулярно расположенных группами (CRISPR), и ассоциированных с ними белков Cas. CRISPR были открыты еще в 1980 году, но разобраться в их функции удалось лишь в 2007-м. Пока идентифицировано три механизма CRISPR; лучше всего изучен тип II. Суть механизма состоит в том, что геном бактериофага или плазмида разрезается на фрагменты, которые включаются в локус CRISPR. При следующем проникновении в клетку тех же ДНК происходит транскрипция локуса с образованием особой crRNA (CRISPR-РНК). Она работает почти как антитела в иммунной системе человека: специфически распознает «враждебный» генетический материал и «натравливает» на него эндонуклеазу Cas. Последняя разрезает ДНК «захватчика» на безопасные фрагменты (рис. 1).
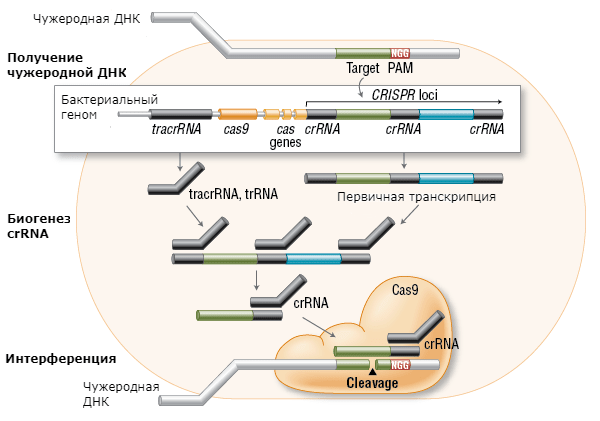
Рисунок 1. Механизм действия системы CRISPR-Cas.
Система рестрикции-модификации
Аналог врожденного иммунитета, обнаруженный учеными у бактерий более полувека назад. В классическом виде она включает два фермента: эндонуклеазу рестрикции (REase) и метилтрансферазу, или метилазу, (MTase). Расправа над бактериофагом происходит следующим образом. Изначально MTase метилирует (присоединяет метильную группу к нуклеотидам) собственную ДНК бактерии в определенных местах — сайтах рестрикции (то есть разрезания эндонуклеазой). Чужой же генетический материал попадает в клетку неметилированным. Далее в дело вступает эндонуклеаза: фермент находит неметилированные сайты рестрикции и вносит в ДНК двухцепочечный разрыв (рис. 2). Получается, как в библейском сюжете, когда ангел поражал египетских первенцев в домах без особого знака на дверях.
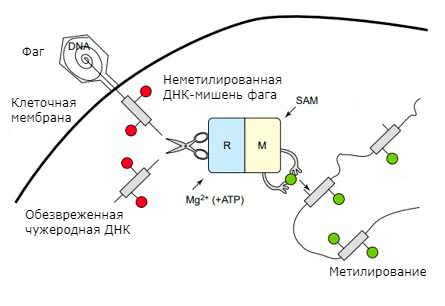
Рисунок 2. Механизм действия системы рестрикции-модификации.
Система абортивной инфекции (Abi)
Своего рода бактериальный «апоптоз». Оказывается, прокариотам не чужд альтруизм. Существует более 20 механизмов, с помощью которых бактериальная клетка убивает себя либо останавливает свой метаболизм, предотвращая распространение инфекции в общей популяции. Система Abi кодируется преимущественно мобильными генетическими элементами, включая плазмиды и профаги.
BREX
Защитный механизм, открытый в 2014 году. Ученые получили из Bacillus cereus генную кассету с шестью генами и интегрировали ее в геном Bacillus subtilis. Донорские гены помогли микроорганизму выработать резистентность к разным видам фагов, как вирулентным, так и умеренным. Предположительно, гены в кассете кодируют домены lon-подобной протеазы, щелочной фосфатазы, РНК-связывающего белка, ДНК-метилазы, АТФазы, а также белок с неизвестной функцией (рис. 3). Система BREX подавляет репликацию фаговой ДНК, не приводя к ее разрушению или деградации.
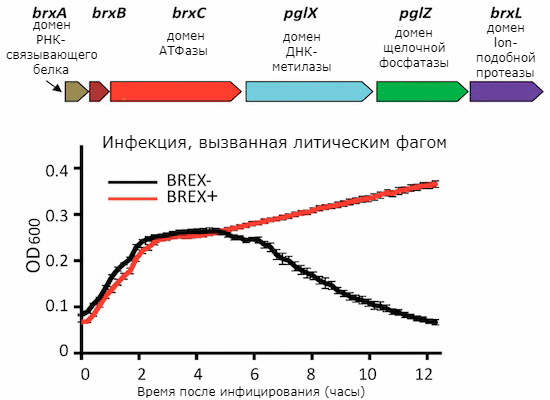
Рисунок 3. Система защиты BREX.
Прокариотические белки Argonaute (pAgo)
Относительно простая и довольно эффективная система защиты бактериальных клеток от чужеродного белка. В эукариотических клетках белки Ago играют ключевую роль в РНК-интерференции. В 2014 году журнал Nature опубликовал статью, в которой ученые сообщали об открытии ДНК-интерференции с участием Ago у прокариот. В ходе изучения микроорганизма Thermus thermophilus было установлено, что, когда в бактериальную клетку проникают чужеродные плазмиды, белок TtAgo образует комплекс с малой интерферирующей ДНК (siDNA) длиной 13–25 нуклеотидов и использует ее для связывания и расщепления комплементарных ей плазмидных ДНК-мишеней. При этом TtAgo умеет различать геномную и «чужую» ДНК. В 2017 году похожие свойства обнаружили у белков PfAgo (Pyrococcus furiosus) и MjAgo (Methanocaldococcus jannaschii).
DISARM
Еще одна недавно открытая защитная система бактерий с не до конца изученным механизмом действия. Известно, что она включает четыре гена, кодирующих ДНК-метилазу, домен фосфолипазы D (PLD), домен хеликазы, домен DUF1998 и еще один ген с неизвестной функцией. DISARM работает по тому же принципу, что система рестрикции-модификации. При переносе DISARM от Bacillus paralicheniformis в Bacillus subtilis система обеспечивала защиту от всех трех семейств «хвостатых» бактериофагов Caudovirales.
Разные бактерии предпочитают использовать разные системы защиты. Так, система рестрикции-модификации есть у 75% прокариот, CRISPR-Cas — у 40%. BREX и pAgo встречаются реже — примерно у 10% бактерий и архей.
ОТВЕТ БАКТЕРИОФАГОВ
Бактерии изобретательны, но и фаги не дремлют. Они постоянно пытаются найти брешь в обороне, создают хитрые механизмы для нейтрализации защиты. И, нужно признать, у них это неплохо получается.
Так, в геномах некоторых бактериофагов закодированы короткие белки, которые подавляют или модулируют работу системы рестрикции-модификации. Атакуя Escherichia coli, фаг P1 впрыскивает в ничего не подозревающую бактерию не только свою ДНК, но и белки DarA и DarB. Они защищают сайты рестрикции фага. Бактериофаг T7 кодирует протеин Ocr, который, маскируясь под ДНК, связывает клеточные эндонуклеазу рестрикции и метилазу. Фаг лямбда использует белок Ral, чтобы вызвать гиперактивацию клеточной метилазы и с ее помощью оперативно обеспечить защиту своего генетического материала от рестрикции (рис. 4).
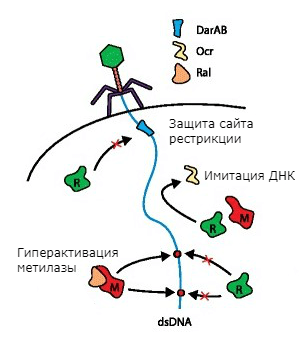
Рисунок 4. Механизмы защиты фагов от системы рестрикции-модификации.
Против системы CRISPR-Cas фаги используют белки анти-CRISPR (Acr). В качестве примера можно привести три белка Acr синегнойного бактериофага, который поражает синегнойную палочку. Эта бактерия использует для самообороны тип I-F системы CRISPR-Cas. Два белка — Acr1 и Acr2 — связываются с комплексом crRNA, не давая ему вступить во взаимодействие с ДНК фага. А белок Acr3 связывается с хеликазой-нуклеазой Cas3, предотвращая деградацию ДНК-мишени (рис. 5).
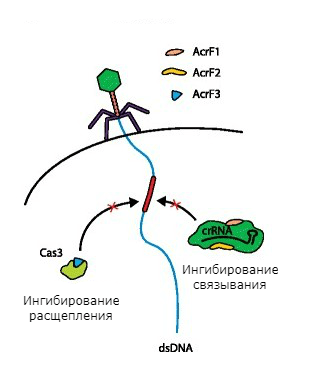
Рисунок 5. Механизмы защиты фагов от системы CRISPR-Cas.
Интересно, что белки Acr обладают высокой степенью специфичности. Они не подавляют «иммунитет» кишечной палочки, которая также использует подтип системы I-F. Не происходит подавления и у синегнойных палочек, использующих другой тип CRISPR-Cas — I-E.
Выяснили, что некоторые фаги обходят и систему BREX. Но какие механизмы они выработали для защиты, еще предстоит изучить.
ТРАНСПЛАНТАЦИЯ ГЕНОВ И БОЖЕСТВЕННЫЕ ИМЕНА
Известно, что гены «иммунной системы» прокариот склонны группироваться на определенных участках генома. Так, гены, кодирующие ферменты рестрикции, часто обнаруживают в окрестностях генов системы абортивной инфекции и других защитных систем. Такие зоны генома называются защитными островками.
Ученые из Института Вейцмана предположили, что на защитных островках есть еще немало белых пятен. Возможно, существуют неизвестные защитные системы, гены которых следуют общей тенденции и находятся в пределах островков.
Для того чтобы проверить свое предположение, ученые исследовали более 14 тыс. семейств белков в 45 тыс. геномов прокариот. После тщательного «кастинга» осталось 335 семейств-кандидатов.
Проверку потенциальных защитных систем решили провести на двух микроорганизмах: Escherichia coli (штамм MG1655) и Bacillus subtilus (штамм BEST7003), в чьих геномах не обнаружили исследуемых генов. Для того чтобы перенесенные гены начали функционировать, в качестве доноров использовали мезофильные микроорганизмы, филогенетически наиболее близкие к реципиентам. Для контроля ученые повторили процедуру с пятью уже известными защитными системами: тремя типами системы рестрикции-модификации, системой абортивной инфекции и системой токсин-антитоксин.
После того как реципиенты получили новые гены, их подвергли атаке «коктейля», в состав которого входили 10 фагов Bacillus subtilus и 6 фагов Escherichia coli. У 9 систем обнаружили способность защищать микроорганизм как минимум от одного бактериофага.
Новые защитные системы назвали в честь богов из разных мифологий. Отдельного внимания заслуживают три из них.
Zorya
Систему назвали в честь славянской богини. Гены этой системы встречаются в бактериальном геноме вблизи генов семейства pfam15611. Система Zorya бывает двух типов. Первый тип (zorABCD) включает 4 гена: zorA, zorB, zorC (собственно, pfam15611, функция которого неизвестна) и zorD. Второй тип (zorABE) лишен генов zorC и zorD, но включает в дополнение к двум первым третий ген zorE. Ученые обнаружили, что гены zorA и zorB содержат домены протеинов, которые показывают отдаленную, но четкую гомологию с доменами в генах motA и motB. Последние кодируют мембранные протеины, которые входят в состав жгутикового двигателя (рис.6).
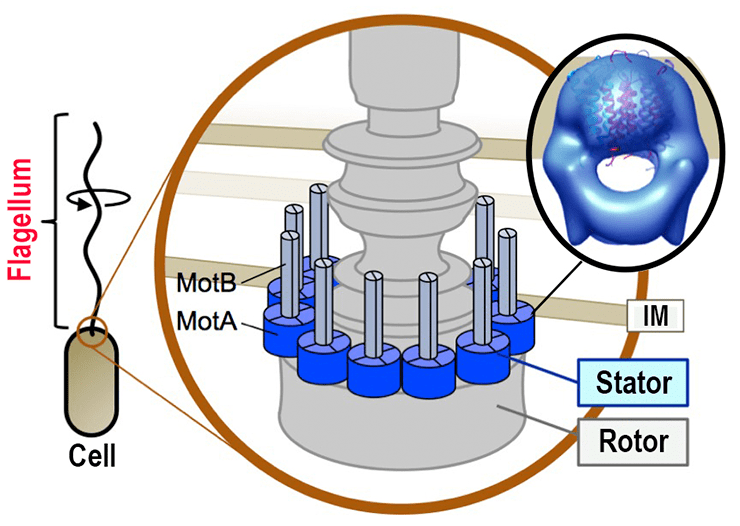
Рисунок 6. Роль протеинов MotA и MotB в составе жгутикового двигателя.
Система MotAB формирует статическую часть, внутри которой вращается жгутик, а также протонный канал, благодаря которому вырабатывается энергия для вращения.
Ученые предположили, что продукты генов zorC, zorD и zorE принимают участие в поиске и инактивации чужеродного генетического материала, а если они не срабатывают, ZorA и ZorB открывают протонный канал, что приводит к деполяризации и гибели клетки. Иными словами, Zorya может работать как разновидность системы абортивной инфекции.
Thoeris
Система получила свое название в честь древнеегипетского бога деторождения и плодородия. Она представлена двумя генами, встречающимися в области pfam08937: thsA и thsB (собственно, включающий pfam08937, также известный как TIR-домен — Toll-интерлейкиновый рецептор). Система Thoeris роднит бактерии с эукариотами: TIR-домен является важной составляющей врожденного иммунитета у растений, беспозвоночных и млекопитающих.
У животных TIR-домен зачастую формирует внутриклеточный компонент связанных с мембраной Toll-подобных рецепторов (рис. 7).

Рисунок 7. Разновидности рецепторов опознавания паттернов в клетках эукариот: TLR — Toll-подобные рецепторы; NLR — Nod-подобные рецепторы; CLR — лектины С-типа; RLR — RIG-I-подобные рецепторы.
Израильские ученые выдвинули гипотезу, согласно которой система Thoeris — это предшественница системы рецепторов опознавания паттернов, представленной в том числе Toll-подобными рецепторами. Рецепторы опознавания паттернов представляют собой белки, которые находятся на поверхности иммунных клеток эукариот и распознают стандартные молекулярные структуры (паттерны) патогенов.
Druantia
Систему назвали в честь галльской богини. Druantia представлена геном, кодирующим очень большой белок, содержащий домен DUF1998 с неизвестной функцией, а также «следы» хеликазы и мотив Walker A/B, указывающий на использование АТФ. Обычно этому большому гену предшествует один из трех типов набора генов, у которых не идентифицированы домены и функции.
Огромный размер системы Druantia говорит о ее сложной функции, а почти полное отсутствие распознаваемых доменов — о том, что она не похожа ни на одну известную защитную систему прокариот.
ЗАЩИТА ОТ ЧУЖЕРОДНЫХ ПЛАЗМИД
Помимо девяти противофаговых, ученые обнаружили у бактерий одну новую систему защиты от плазмид. Ее назвали Wadjet — по имени древнеегипетского божества. Все три известных типа системы представлены четырьмя генами: jetA, jetB, jetC и jetD. Оказалось, что первые три имеют структурную гомологию с генами конденсинов MukF, MukE и MukB. Конденсины отвечают за организацию и расхождение хромосом при делении клетки.
Ученые выдвинули гипотезу о том, что гены jetABC произошли от mukBEF и стали специализироваться на защитной функции. Возможно, их продукты, используя свои свойства конденсинов, препятствуют правильной сегрегации чужеродных плазмид и тем самым предотвращают их передачу дочерним клеткам.
ПЕРСПЕКТИВЫ
Точка в изучении бактериально-фаговой гонки вооружений не поставлена. Скорее, у исследователей из Института Вейцмана получилось большое многоточие. Наверняка известны еще далеко не все защитные системы бактерий. Некоторые из них по тем или иным причинам могли не проявить себя в ходе исследования: ведь даже уже известные защитные механизмы, которые ученые использовали для контроля, оказались эффективны лишь в половине случаев.
Кто знает, может быть, настанет день, когда будет открыта очередная защитная система прокариот, и с ее помощью удастся совершить переворот в молекулярной биологии, в тени которого затеряется даже слава знаменитой CRISPR-Cas.
Источник: БИОМОЛЕКУЛА

