Всякий раз, когда мы говорим о стволовых клетках, обязательно упоминаем про их медицинские перспективы. Как известно, стволовые клетки могут превращаться в любой другой тип клеток, и с их помощью вполне можно было бы восполнять клеточные потери, случающиеся при травмах, болезнях и т. д.
Знаменитые нейродегенеративные болезни (болезнь Альцгеймера, Паркинсона и т. д.) связаны как раз с массовой гибелью нейронов в мозге. Раз стволовые клетки превращаются во что угодно, значит, и в нейроны тоже. Можно ли с помощью клеточно-стволовых методов добавить мозгу нервных клеток взамен погибших?
Здесь есть один очень важный момент – новый нейрон ведь недостаточно просто засунуть в мозг, он должен установить контакты с другими нервными клетками, включиться в нейронные цепочки, которые обрабатывают ту или иную информацию. Может ли пересаженный нейрон все это проделать? Нас самом деле может: год назад мы писали про эксперименты, в которых нейроны, полученные из стволовых клеток, пересаживали мышам в мозг, в зрительную кору – пересаженные клети установили правильные контакты с «местными», так что зрение у мышей даже улучшилось.
Исследователи из Университета Киото проделали нечто похожее с обезьянами, только на сей раз речь шла о том, чтобы внедрить в мозг нейроны иной разновидности – те, которые в первую очередь гибнут во время синдрома Паркинсона.
Для этого использовали искусственные стволовые клетки, которые получают из зрелых специализированных клеток тела: у семи человек (трех с болезнью Паркинсона и четырех здоровых) брали образцы крови и кожи и затем с помощью специального белкового коктейля перепрограммировали кожные и кровяные клетки так, чтобы они утратили специализацию, забыли про свои функции и вернулись, так сказать в детство.
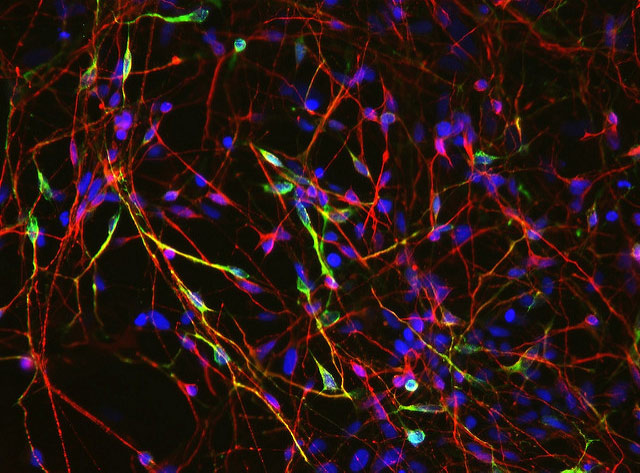
Нейроны, выращенные из эмбриональных стволовых клеток; желтым цветом окрашены нервные клетки, синтезирующие дофамин.
Полученные таким образом индуцированные плюрипотентные стволовые клетки, как и настоящие стволовые клетки из эмбриона, способны делиться чрезвычайно долго, так что их можно было нарастить в нужном количестве, а потом с помощью уже других белков-регуляторов отправить на нейронный путь развития.
Нейроны, как мы сказали, нужны были не любые, а те, которые синтезируют дофамин и работают в двигательных центрах мозга (болезнь Паркинсона, как известно, сказывается в первую очередь на координации движений).
Клетки, когда специализируются, проходят через несколько этапов. Исследователи дожидались, когда стволовые клетки до определенного момента продвинутся в своих превращениях в нервные клетки, после чего пересаживали их в мозг макак-крабоедов, где клетки окончательно превращались в зрелые нейроны двигательной коры.
Макакам же перед клеточной пересадкой вводили специальный нейротоксин, который убивал двигательные нейроны в мозге, так что у обезьян начинались симптомы, похожие на симптомы болезни Паркинсона. Но после того, как у них в мозге появлялись новые клетки, состояние обезьян улучшалось на 40–50%: так, характерный тремор конечностей у них становился не таким сильным, как раньше, движения животных становились более естественными.
Терапевтический эффект был долговременным, он длился как минимум год. То есть пересаженные клетки не только успешно дозрели до дофаминовых нейронов, они сумели включиться в работу нервных цепочек – хотя, как пишут исследователи в статье в Nature, такие нейроны по сравнению с природными клетками синтезировали только половину того дофамина, что должны были. (Возможно, если бы клетки на замену удалось заставить давать больше дофамина, то и лечебный эффект был бы сильнее.)
Стоит напомнить, что клеточное сырьё для экспериментов брали в том числе и у людей с синдромом Паркинсона, тем не менее, никаких проблем с такими клетками не возникло. Даже если причины болезни у тех людей были наследственно-генетические – а это значит, что соответствующие дефектные гены были у всех клеток организма – то все равно они никак не проявились ни после превращения в стволовые клетки и затем в нейроны, ни после пересадки в обезьяний мозг.
И все же, если говорить о будущих клинических перспективах, то желательно все-таки больному человеку пересаживать клетки, полученные от здорового донора. И тут возникает проблема с иммунитетом, который должен атаковать чужие клетки.
Однако тут можно воспользоваться некоторыми уловками, которые описаны в параллельной статье в Nature Communications. Иммунные клетки отличают своих от чужих по особым молекулам на клеточной мембране, и подбирая донора, нужно постараться найти такого, чтобы мембранные молекулы на его клетках были похожи на мембранные молекулы на клетках больного.
Как показали опыты на тех же обезьянах, это действительно позволяет до некоторой степени усыпить бдительность иммунной системы. Впрочем, хотя тут еще предстоит выполнить массу исследований на тему безопасности и надежности метода, важно, что клеточно-стволовой подход в принципе может помочь в случае конкретных заболеваний нервной системы.
Конечно эффект мог быть и от того что убитые иммунитетом нейроны синтезировавшие дофамин выделяли сигналы которые заставляли собственные стволовые клетки макак-крабоедов замещать погибшие ранее нейроны. Но в любом случае работа интересна методом получения плюрипотентных клеток.
Источник: НАУКА И ЖИЗНЬ

