SPC3649 или Миравирсен – лекарство нового поколения против гепатита С.
20 лет прошло с момента открытия первой микроРНК. Еще немногим раньше, в 1989 году, люди научились диагностировать гепатит С, часто называемый «ласковым убийцей». «И как же связаны эти два события?» — спросите вы. А связь в том, что лекарство нового поколения Миравирсен, чей принцип действия основан на знаниях о микроРНК, будет излечивать людей от этого страшного вируса. Но как исследователи смогли создать такой препарат?
Открытие
Ровно 20 лет назад, в 1993 году, Виктор Амброс и Гэри Рувкин открыли первый ген микроРНК (или на английском miRNA) lin-4 в геноме нематоды C. elegans, а также показали, что мутация по этому гену приводит к нарушению развития червя во взрослое животное. Их статьи опубликовали в одном номере журнала Cell. Долгое время lin-4 считался неясной аномалией генома, пока в 2000 году не обнаружили малую регуляторную РНК let-7. Искусственного заблокировав функции let-7, можно получить червей, у которых не происходит формирования энтодермы при одновременной активации формирования мезодермы и эктодермы из эмбриональных стволовых клеток. С этого момента исследователи окончательно осознали, что микроРНК не просто транскрипционный «шум», а важный регулятор в клетке, и занялись поиском аналогичных элементов в геномах дрозофилы, человека и т.д. К 2011 году у животных, растений и вирусов было аннотировано 18226 микроРНК, включая 1921 в человеческом геноме . Не правда ли, неплохой результат за 10 лет исследований?

Рисунок 1. Общая формула LNA — locked nucleic acid. При замене X на кислород, а Y — на серу, получают так называемые фосфоротиоатные «закрытые» нуклеотиды.
Locked nucleic acid
Вот небольшое отступление, касающееся инструментов, которые используются в работе с микроРНК. В 1998 году исследователь Кошкин добавил к инструментарию молекулярной биологии технику создания «закрытых» нуклеиновых кислот (LNA — lockednucleicacid). Что же кроется за этим названием?
LNA — это бициклический аналог РНК, рибозное кольцо которого находится в C3’-эндо конформации, благодаря появлению 2’-O,4’-C метиленового мостика (рис. 1).
Модифицированные таким образом нуклеотиды демонстрируют высокие термостабильность и сродство в дуплексе с целевыми молекулами РНК.
LNA очень специфичны в вопросе «отлавливания» малых РНК, в частности, микроРНК.
В последующие годы ученые активно использовали LNA в нозерн-блоттинге, insitu-гибридизации, а также whole-mountinsitu-гибридизации, что привело в 2006 году к появлению такого термина как antimiR. АнтимиР-ами были названы LNA-аналоги антисмысловых олигонуклеотидов, способные ингибировать функцию микроРНК в культуре клеток. В основе этого ингибирования лежит принцип Уотсон-Криковских взаимодействий.
И вот, к 2005 году стало ясно, что информации о микроРНК накопилось достаточно для того, чтобы приступить к созданию лекарства следующего поколения. Во-первых, результаты исследований явно указывали, что нарушения регуляции микроРНК ведут к заболеваниям*. Во-вторых, успешное применение технологии «закрытых» нуклеиновых кислот обеспечит практически беспроблемный дизайн антимиРНК-олигонуклеотидов для фармакологического ингибирования нужных микроРНК invivo. Почему практически? Под вопросом оставался сущий пустяк: как осуществить доставку в желаемое место в организме?
* — Например, ослабление функций miR-14 существенно увеличивает общее содержание триацилглицеридов; miR-278 осуществляет контроль продукции инсулина, а делеция miR-278 стимулирует данный процесс; повышенная экспрессия miR-1, специфичной для сердца, ингибирует кардиомиоциты во время его эмбриогенеза и провоцирует аритмогенез.
Тут внимание исследователей привлекает miR-122:
miR-122 отличается не только полной консервативностью у всех позвоночных от рыбок Данио до человека, но и высокой концентрацией в печени;
также ученые вспомнили, что антимиРНК олигонуклеотиды с фосфоротиоатным (PS) каркасом накапливаются опять же в печени, причем для этого не нужны никакие дополнительные модификации;
кульминационным аккордом стало сообщение Питера Сарнова в 2005 году, что экспрессированная в печени miR-122 взаимодействует с РНК вируса гепатита С. Все факты говорили о том, что miR-122 — важнейший внутренний фактор размножения гепатита С.
Вот так зародилась идея по созданию первого в мире лекарства на основе микроРНК, которое поможет излечиться 170 миллионам людей, зараженным гепатитом С. С этого момента началась история создания Миравирсена.
В двух словах про гепатит С
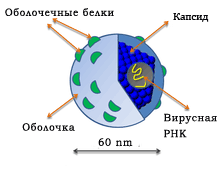
Рисунок 2. Строение вирусной частицы гепатита С.
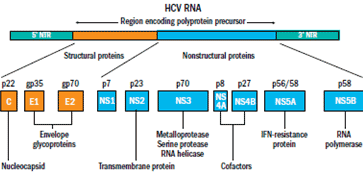
Рисунок 3. Структура генома вируса гепатита C. Геном состоит 5’- и 3’-НТО и областей со структурными (C, E1, 2) и неструктурными (NS1, 2, 3, 4A,4B, 5A, 5B) белками. Особый интерес для исследователей представляют 5’-НТО и NS3, 4A.
Этиология
Впервые вирус гепатита С был обнаружен в 1989 году. По классификации он принадлежит к роду Hepacivirus семейства Flaviviridae. Представляет собой маленький (40-60 нм в диаметре), оболочечный, одноцепочечный, +РНК вирус. Состоит из РНК, помещенной в икосаэдрический белковый капсид, который, в свою очередь, защищен липидной оболочкой (рис. 2). Геном вируса состоит из единственной открытой рамки считывания длиной примерно 9600 п.н.о. (рис. 3). Известно 6 генотипов с подтипами и квазивидами гепатита С. Распространение того или иного вида зависит от географического расположения.
Эпидемиология
По данным ВОЗ, более 170 миллионов человек инфицированы гепатитом С, что составляет 3% всего населения Земли. Чаще всего вирус гепатита С передается при воздействии инфицированной крови. Это может происходить следующими путями (информация с сайта ВОЗ):
при переливании зараженной крови и продуктов крови и при пересадке органов;
при инъекциях загрязненными шприцами и травмах от укола иглой в медицинских учреждениях;
при употреблении инъекционных наркотиков;
новорожденному ребенку от инфицированной гепатитом С матери.
Гепатит С может передаваться при сексуальных контактах с инфицированным человеком или при совместном пользовании личными предметами, загрязненными инфицированной кровью, но это происходит реже.
гепатит С не передается с грудным молоком, через пищевые продукты или воду и при безопасных контактах, таких как объятия, поцелуи или совместное употребление в пищу продуктов и напитков с инфицированным человеком.
Острое инфекционное состояние. Во время острой фазы, которая длится около полугода, у 60–70% инфицированных не развивается никаких симптомов, что затрудняет своевременную постановку диагноза. 15–25% инфицированных смогут избавиться от вируса самостоятельно, у остальных гепатит С перейдет в хроническую стадию. Хроническое состояние также бессимптомно, пока не станут заметны явные повреждения в печени. В итоге болезнь обнаруживают, когда пациент страдает от цирроза, рака печени или вовсе полного отказа органа. Поэтому в народе гепаптит С окрестили «ласковым убийцей». По данным эпидемиологических исследований на гепатит С вместе со своим «собратом» гепатитом В приходится ¾ всех болезней печени.
Лечение
Золотым стандартом лечения на данный момент принят пегинтерферон-α (интерферон-α+полиэтиленгликоль) в комбинации с рибавирином. Из побочных эффектов: зуд, заложенность носа. Основные проблемы пегинтерферонов и рибавирина — это высокая заболеваемость, симптомы как при гриппе, усталость. Такие побочные эффекты, конечно, никому не нравятся, так как снижают качество жизни, работоспособность. Люди часто отказываются от лечения, особенно в бессимптомный период, что сводит возможность выздоровления к минимуму.
Но арсенал фармацевтических компаний этим не исчерпываются. В 2011 году на рынок поступили новые препараты: ингибиторы вирусной протеазы NS3/4AIncivek® (телапревир) и Victrelis® (боцепревир). Протеазные ингибиторы могут служить субстратами для цитохрома Р-450, а такие «пересечения» в метаболических цепочках приводят к нежелательным взаимодействиям между веществами. Само по себе создание и производство подобной протеазы было задачей непростой и дорогостоящей. Для нашей страны цена препарата неподъёмная: курс телапревира стоит 250 тысяч рублей! И завершающая ложка дегтя: эти препараты вызывают анемию, что очень отдаляет их от идеала.
Миравирсен. Доклинические исследования
Миравирсен (продукт компании SantarisPharma) представляет собой LNA-antimiRNA олигонуклеотид, которому присвоено название miravirsensodium(соль натрия — желтовато-белый гигроскопичный порошок). Его состав — восемь D-oxy-LNA и семь ДНК-нуклеотидов в следующей последовательности: 5’-mC-c-A-t-t-G-T-c-a-mC-am-C-t-mC-mC-3‘ (заглавные буквы — LNA, строчные — ДНК).
Молекулярная формула C151H171N49Na14O83P14S14
Молекулярный вес 5204.65 г/моль
Название молекулы SPC3649
miRNA-122 — самая распространенная микроРНК в гепатоцитах — регулирует образование энергии, липидный и стероидный обмен и репликацию гепатита С. miRNA-122 — жизненно важный фактор для вируса: без нее гепатит С не способен эффективно размножаться. Интересный факт: если сделать инъекцию miRNA-122 в негепатоцитные клетки, то вирус гепатита С станет реплицироваться и там.
Как же miRNA-122 взаимодействуют c геномом гепатита С? Известно, что +РНК вируса содержит два практически идентичных сайта — S1 и S2, — расположенные в 5’-нетранслируемой области (НТО) вирусного генома (рис. 4А). Они связываются с двумя miR-122, и образовавшийся комплекс защищает вирусную РНК от нуклеаз и иммунной системы в гепатоцитах (рис. 4В). Сайты для связывания miR-122 сохраняют свою консервативность среди всех известных генотипов и подтипов гепатита С.
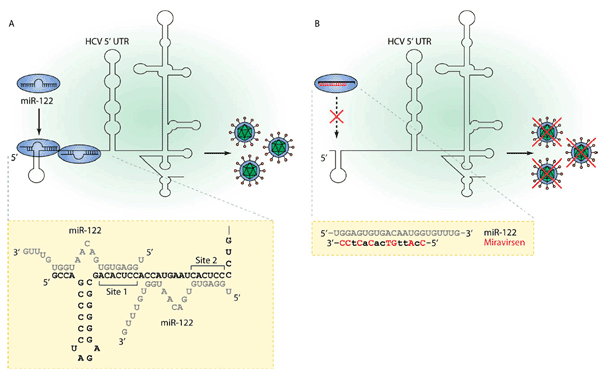
Рисунок 4. Механизм действия miR-122 и Миравирсена. А. В 5’-НТО генома гепатита С расположены два сайта, комплементарные miRNA-122, — S1 и S2. С ними и взаимодействует микроРНК, стимулируя репликацию. В. Миравирсен образует комплекс с miRNA-122, которая таким способом становится недоступной вирусу.
Миравирсен синтезирован таким образом, чтобы специфически подавлять miRNA-122, образуя дуплекс. Как только miRNA-122 становится недоступной для вируса, его распространение полностью подавляется.
Окончательный вариант формулы появился не сразу. Во-первых, создали небольшую библиотеку олигонуклеотидов длиной 13–16 нт с минимальной температурой плавления 60 °С. Во-вторых, исключили комплементарность первого нуклеотида микроРНК, так как исследования показали, что этот нуклеотид «прячется» в особом сайте белка Argonaute. В-третьих, чтобы предотвратить возможное разрезание комплексом RISC (RNA-inducedsilencingcomplex) потенциальных сайтов, были введены замены на LNA-нуклеотиды. Не забыли и про PS-скелет и комплементарность 5’-НТО вирусного генома. После экспериментов на человеческих линиях клеток гепатотоцитов в лидеры вышел олигонуклеотид под названием SPC3649. Именно SPC3649 вошел в историю под названием Миравирсен.
Первым делом новый препарат испробовали на мышах, и весьма успешно. Животным вкалывали внутрибрюшинно от 12,5 до 75 мг/кг/доза два раза в неделю и через четыре недели достигли ингибирования miRNA-122. Тем временем исследователи обратили внимание, что параллельно с miRNA-122 в плазме крови снижается уровень холестерина (на 30–40%) и сочли, что это очень удобный биомаркер. Исследования на животных и некоторых приматах не выявили побочных эффектов. Итак, краткосрочное ингибирование miRNA-122 было признано безопасным.
Другие «олиги»
Миравирсен далеко не уникальный в своем роде лекарственный препарат. В разработке сейчас находится еще десяток олигонуклеотидов, чей принцип действия основан на ингибировании соответствующих микроРНК. Например, Мипомерсен ингибирует экспрессию аполипопротеина В-100 в печени и применяется в лечении семейной гиперхолестеринемии.
Миравирсен. Клинические исследования
В 2010 году канадская фармацевтическая компания SantarisPharmaA/S приступила к клиническим испытаниям на пациентах, инфицированных гепатитом С. По данным от мая 2013 года Миравирсен™ находится на стадии IIa клинических испытаний. Уже известно, что у четырех из девяти пациентов после курса инъекций Миравирсена РНК вируса в крови не обнаруживалась (рис. 5); серьезных побочных эффектов при этом не выявлено. Предполагается, что препарат будет необходимо принимать раз в несколько недель.
По оценкам маркетологов, цена лекарства будет доступной благодаря простоте LNA-технологий. С их помощью можно синтезировать вещество в больших количествах и дешево. К 2018 году ожидается настоящая сенсация, когда Миравирсен™ появится на полках аптек.
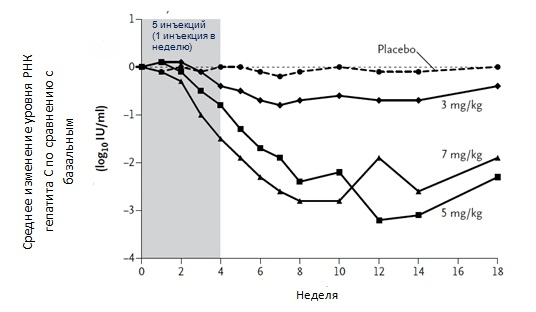
Рисунок 5. Клинические испытания Миравирсена. На графике представлены четыре группы пациентов, принимавших участие в клинических испытаниях: плацебо, 3, 5 и 7 мг/кг. Хорошо заметны: а) положительная динамика при высоких концентрациях и б) падение титра вирусной РНК.
Источник: БИОМОЛЕКУЛА



