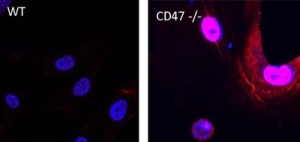
Усиленная пролиферация и снижение скорости старения CD47-нулевых мышиных эндотелиальных клеток связаны с повышенной экспрессией с-Мус. На снимке экспрессия с-Мус (окрашен красным) в WT и CD47−/− эндотелиальных клетках. Синим окрашены ядра. (Scientific Reports)
Ученые Школы медицины Университета Питтсбурга (University of Pittsburgh School of Medicine) и Национальных институтов здоровья США (National Institutes of Health, NIH) доказали, что тканеспецифические и стволовые клетки можно получать из зрелых клеток млекопитающих путем блокирования одного из мембранных белков. Как показывают результаты их экспериментов, опубликованные в журнале Scientific Reports, этот процесс не требует присутствия других видов клеток или агентов для искусственного поддержания их роста и не активирует раковые гены.
По словам соавтора исследования адъюнкт-профессора Школы медицины Джеффри Айзенберга (Jeffrey Isenberg), MD, ученые надеются, что стволовые клетки, выращенные в лаборатории, и индуцированные плюрипотентные стволовые клетки, способные стать специализированными клетками определенных тканей, например, нейронами или кардиомиоцитами, однажды будут использоваться для лечения болезней и восстановления поврежденных тканей.
«Хотя стволовые клетки способны к самообновлению, их довольно сложно вырастить в лаборатории», - объясняет ученый. «Чтобы искусственно создать условия, необходимые для их выживания и хорошего роста и размножения, часто приходится использовать фидерные клетки или вирусные векторы».
В 2008 году, работая в лаборатории Дэвида Робертса (David Roberts), PhD, в Национальном институте рака (National Cancer Institute, NCI), доктор Айзенберг изучал влияние на кровеносные сосуды соединений, блокирующих мембранный белок CD47. Он заметил, что, если клетки слизистой оболочки легких – эндотелия – подвергались воздействию одного из блокаторов CD47, они остаются здоровыми и сохраняют способность расти и функционировать в течение нескольких месяцев.
CD47 — поверхностный клеточный гликопротеин, играющий роль в межклеточном взаимодействии, предотвращает захват нормальных эритроцитов фагоцитарными клетками. Лиганд рецептора SIRPA (SIRPα, CD172a). CD47 играет роль в клеточной адгезии, являясь рецептором для тромбоцитарного THBS1, и в модулировании интегринов. Играет важную роль в формировании памяти и синаптической пластичности в гиппокампе. CD47 является лигандом рецептора SIRPA (SIRPα), связывание с которым блокирует созревание незрелых дендритных клеток и ингибирует образование цитокинов зрелыми дендритными клетками. Взаимодействие с другим рецептором SIRPG способствует межклеточной адгезии. Предотвращает клиренс из крови нормальных эритроцитов.
В марте 2012 года были опубликованы результаты исследования, согласно которым CD47 препятствует фагоцитозу раковых клеток. Блокирование взаимодействий CD47—SIRPα антителами к CD47 позволило уменьшить лейкосаркому у мышей.
Группа доктора Робертса в NCI продолжила эксперименты с блокированием CD47, уделив основное внимание молекулярным механизмам, лежащим в основе его способности контролировать рост клеток.
Ученые установили, что, в отличие от клеток контрольных мышей, эндотелиальные клетки животных с отсутствием CD47 быстро размножались и росли в культуре. Как оказалось, причиной этому было усиление экспрессии четырех генов, которые считаются необходимыми для образования плюрипотентных стволовых клеток. При помещении в определенную ростовую среду лишенные CD47 клетки спонтанно образовывали характерные для плюрипотентных клеток кластеры, а добавление к культуральной среде различных факторов роста позволяло направить их дифференциацию в сторону клеток других типов тканей. Несмотря на бурный рост, они не образовывали опухолей при введении мышам – основная опасность, сопряженная с использованием индуцированных плюрипотентных стволовых клеток.
«Полученные этим новым способом стволовые клетки должны быть намного безопаснее для пациентов», - отмечает доктор Робертс. «Кроме того, этот метод делает возможным лечения различных заболеваний путем введения препарата, стимулирующего размножение собственных стволовых клеток пациента».
По словам доктора Айзенберга, эти эксперименты показывают, что можно взять первичную клетку человека или других млекопитающих, даже зрелую взрослую клетку, и путем таргетинга CD47 активировать ее потенциал плюрипотентности. Таким образом можно получить клетки мозга, печени, мышц и любые другие. В краткосрочной перспективе они могли бы дать определенный толчок целому ряду лабораторных исследований.
В будущем методы, основанные на блокировании CD47, позволяющие получать большие количества здоровых клеток для клинического применения, могут стать альтернативой традиционной трансплантации костного мозга и сложной биоинженерии органов и тканей, добавляет ученый.
«Эти захватывающие результаты являются обоснованием использования методов блокирования CD47 для усиления накопления и повышения выживаемости стволовых клеток в пересаженных органах и матричных трансплантатах», - комментирует статью профессор Марк Глэдвин (Mark Gladwin), MD, руководитель отделения пульмонологии, аллергологии и реаниматологии Школы медицины. «Это продолжение тесного и продуктивного сотрудничества между учеными NCI и Института сосудистой медицины Университета Питтсбурга».
Источник: LifeSciencesToday

